„Wojna z rakiem”, ogłoszona ponad 50 lat temu, miała na celu całkowite wyeliminowanie tej choroby. Obiecywano nam przełomy, które odmienią medycynę. Tymczasem, choć postęp jest widoczny – na przykład w postaci poprawy pięcioletnich wskaźników przeżycia – jesteśmy dalecy od ostatecznego zwycięstwa. W przypadku chorób takich jak Alzheimer sytuacja jest jeszcze gorsza; przez 20 lat nie pojawił się żaden nowy lek, a te zatwierdzone w ostatnim czasie mają marginalne efekty.
To rodzi fundamentalne pytanie: dlaczego? Dlaczego, mimo ogromnych inwestycji i geniuszu tysięcy naukowców, postęp w naukach biomedycznych wydaje się tak powolny? Istnieją dwie główne narracje. Pierwsza, bardziej pokorna, mówi, że biologia jest po prostu zbyt skomplikowana. Systemy biologiczne, ukształtowane przez miliony lat ewolucji, są niezwykle złożone, chaotyczne i nieprzewidywalne, co ogranicza skuteczność naszych interwencji. Druga, bardziej arogancka, głosi, że to problem talentu. Zwolennicy tej teorii, tacy jak Peter Thiel, sugerują, że najtęższe umysły wybierają „twardsze” nauki, takie jak fizyka czy matematyka, pozostawiając biologię w rękach ludzi, którzy „nie byli wystarczająco dobrzy z matmy”.
Ta druga teza, choć prowokacyjna, jest głęboko myląca i odwraca uwagę od prawdziwych problemów. To nie brak talentu matematycznego hamuje biologię. Prawdziwym wąskim gardłem jest coś zupełnie innego.
Genomics: studium przypadku, czyli matematyka kontra bałagan
Historia genomiki jest idealnym studium przypadku, aby obalić tezę o „braku talentu”. Genomika to dziedzina, która od samego początku była przesiąknięta duchem matematyki i informatyki. Jej celem było „zdigitalizowanie” biologii, sprowadzenie jej do „kodu” – genomu składającego się z czterech liter.
-
Napływ talentów: Genomika przyciągnęła wielu wybitnych naukowców z wykształceniem matematycznym i fizycznym, takich jak Eric Lander, Aviv Regev czy Richard Durbin, którzy stali się liderami w tej dziedzinie, kierując największymi inicjatywami i osiągając ogromny wpływ, także poza światem akademickim.
-
Ogromne zasoby: Projekty takie jak Human Genome Project czy ENCODE (mapowanie epigenomu) otrzymały gigantyczne finansowanie i status priorytetowych, a ich ukończenie ogłaszali prezydenci, co jest rzadkością w biologii.
-
Technologiczny skok: W ciągu 30 lat przeszliśmy od żmudnego poszukiwania pojedynczego genu (jak BRCA2, odpowiedzialnego za raka piersi) do rutynowego sekwencjonowania całych genomów za kilkaset dolarów. To gigantyczny postęp technologiczny.
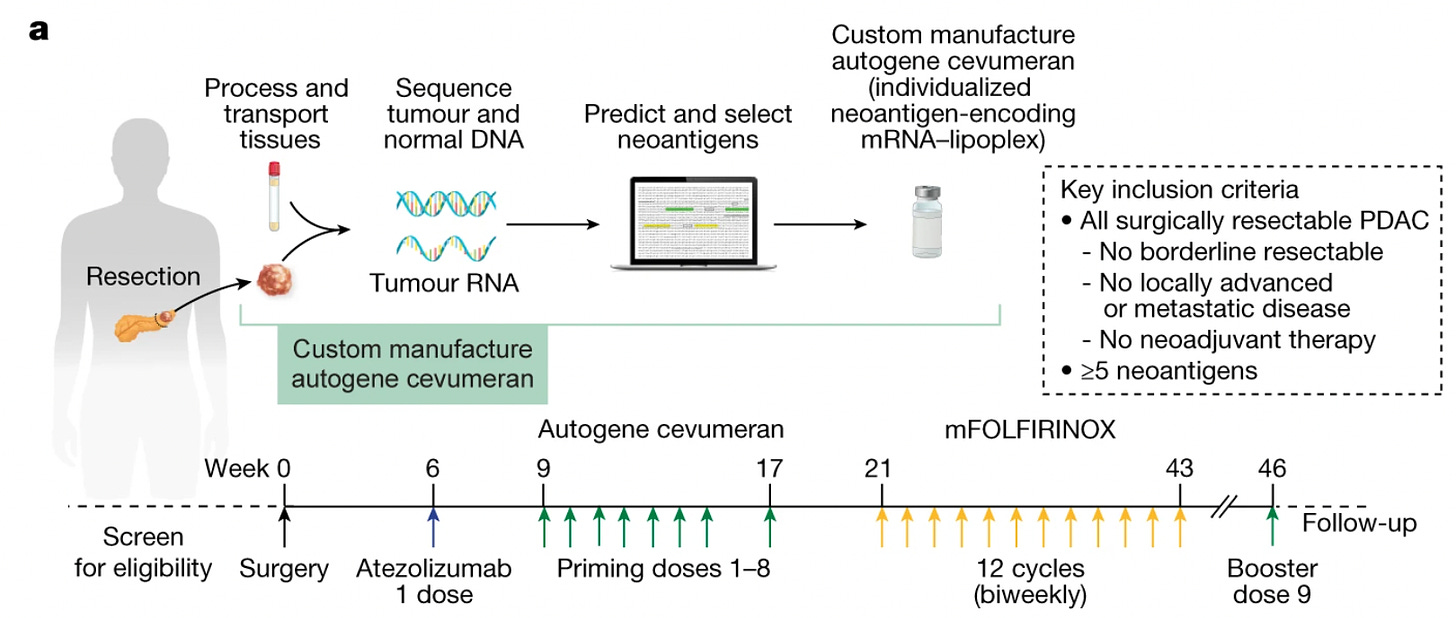
Mimo to, rewolucja w medycynie, którą obiecywano, nie nadeszła. Oczywiście, mamy postępy: spersonalizowane szczepionki mRNA na raka czy leki celowane genomowo, ale działają one u mniejszości pacjentów. Samo odczytanie „księgi życia” nie wystarczyło. Dlaczego?
Bo biologia jest skomplikowana.
-
Genom to nie wszystko: Odkrycie, że człowiek ma tyle samo genów co prosty robak (C. elegans), było szokiem. Szybko stało się jasne, że złożoność organizmu nie wynika tylko z liczby genów. Kluczowa jest epigenetyka – chemiczne „znaczniki” na DNA, które decydują, które geny są włączone, a które wyłączone w danej komórce.
-
Epigenetyka to nie wszystko: Kiedy nauczyliśmy się mapować te znaczniki na masową skalę (projekt ENCODE), okazało się, że nasza wiedza o ich funkcji jest wciąż powierzchowna. Eksperymenty, w których sztucznie wprowadzano metylację DNA (która miała wyciszać geny), pokazały, że połowa genów zachowuje się w nieoczekiwany sposób – nie zmieniając ekspresji lub nawet ją zwiększając. Odpowiedź naukowców? „Odpowiedzi transkrypcyjne na metylację DNA są wysoce zależne od kontekstu.”
-
Nowotwór to ruchomy cel: Nawet jeśli zidentyfikujemy mutację napędzającą raka i stworzymy na nią lek, guz potrafi błyskawicznie ewoluować, nabywając nowe mutacje i uciekając przed terapią.
W każdym z tych przypadków potężne narzędzia matematyczne i obliczeniowe zderzyły się z fundamentalną cechą biologii: jej chaotyczną, kontekstową i ewolucyjną naturą. To nie brak matematyki jest problemem, ale sama istota żywych systemów.
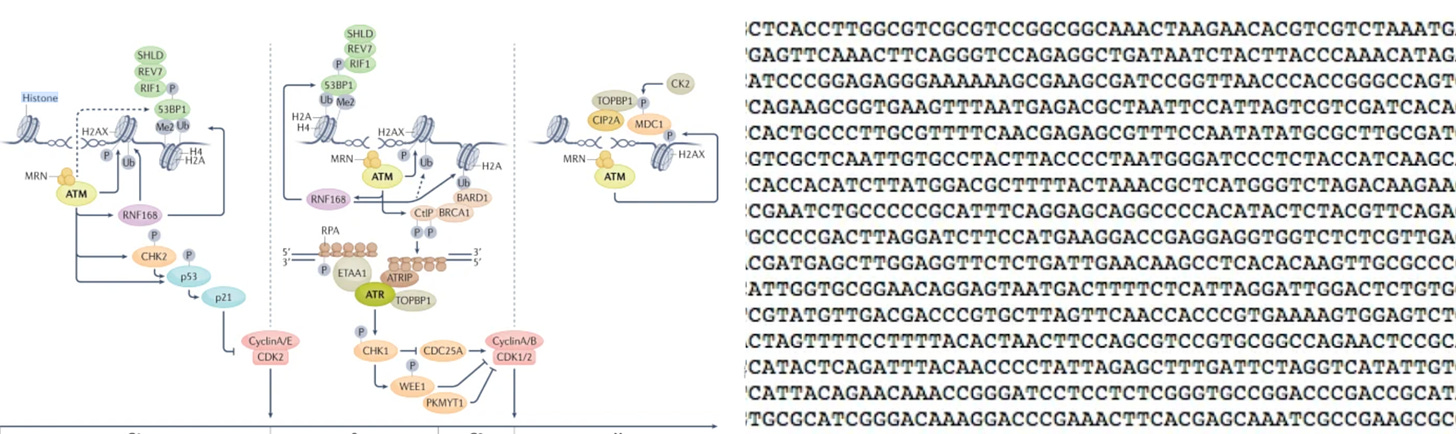
Prawdziwe wąskie gardło: szybkość pętli sprzężenia zwrotnego
Jeśli nie talent, to co jest głównym czynnikiem ograniczającym postęp? Odpowiedź brzmi: długie pętle sprzężenia zwrotnego (ang. long feedback loops).
W fizyce możemy przewidzieć wiele zjawisk z pierwszych zasad. W biologii, ze względu na jej ewolucyjną historię, jesteśmy skazani na iteracyjne cykle eksperymentów: hipoteza -> test -> wynik -> nowa hipoteza. Postęp zależy od tego, jak szybko możemy przejść przez ten cykl.
-
W naukach podstawowych: Postęp jest stosunkowo szybki. Dzięki nowym technologiom, takim jak eksperymenty multipleksowe (gdzie testujemy tysiące zmiennych naraz), możemy przyspieszać te cykle. Firmy takie jak Dyno Therapeutics wykorzystują tę strategię, iteracyjnie projektując i testując tysiące wariantów białek, aby znaleźć te najlepsze do terapii genowej.
-
W medycynie: Pętle sprzężenia zwrotnego są dramatycznie powolne. Sprawdzenie, czy lek działa na ludzi, wymaga dekady badań przedklinicznych i klinicznych. 90% leków, które wchodzą do badań na ludziach, ostatecznie okazuje się nieskuteczna. Każda porażka, a zwłaszcza poważny efekt uboczny (jak śmierć Jessego Gelsingera w 1999 roku, która zamroziła rozwój terapii genowej na lata), zniechęca inwestorów i cofa całą dziedzinę o dekady.
Co gorsza, te pętle w medycynie stają się coraz wolniejsze i droższe. Badania kliniczne kosztują coraz więcej, co oznacza, że za te same pieniądze można ich przeprowadzić mniej. Jednocześnie, trendy polityczne, takie jak regulowanie cen leków (np. Inflation Reduction Act w USA), mogą prowadzić do zmniejszenia inwestycji w badania i rozwój. Mamy więc do czynienia z toksyczną kombinacją: coraz wolniejszych i droższych badań przy jednoczesnym spadku finansowania.
Przyszłość: optymizm dla biologii, pesymizm dla medycyny?
Mając na uwadze powyższe, można sformułować ostrożną prognozę:
-
Przyszłość biologii wygląda optymistycznie. Szybkość eksperymentowania w laboratoriach rośnie. Nowe techniki i automatyzacja pozwalają na coraz szybsze testowanie hipotez. Jest to w dużej mierze oddolny, emergentny proces napędzany przez tysiące naukowców.
-
Przyszłość medycyny wygląda mniej różowo. Spowalniające pętle sprzężenia zwrotnego w badaniach klinicznych, rosnące koszty i presja na obniżanie cen leków mogą zahamować postęp. Jeśli te trendy się utrzymają, jedyną nadzieją jest to, że biologia podstawowa stanie się tak dobra, że kandydaci na leki wchodzący do badań klinicznych będą mieli znacznie większe szanse powodzenia.
Biologia to nie sztuka optymalizacji, jak fizyka. To sztuka tego, co satysfakcjonujące, co działa wystarczająco dobrze, aby przetrwać. Naszym zadaniem nie jest narzekanie na brak talentów matematycznych, ale budowanie systemów – zarówno w laboratorium, jak i w polityce zdrowotnej – które pozwolą nam uczyć się na błędach tak szybko, jak to tylko możliwe. To właśnie skrócenie pętli sprzężenia zwrotnego, a nie poszukiwanie mitycznych geniuszy, jest kluczem do wygrania wojny z rakiem i innymi chorobami.
Dlaczego wciąż nie wyleczyliśmy raka? To nie wina biologów. Prawdziwy problem leży gdzie indziej. by www.doktoraty.pl